Công thức tính số loại phân tử được hình thành từ các loại đồng vị - Hóa học 10 chân trời sáng tạo 1. Kiến thức nền tảng cần nhớ Đồng vị là ...
Công thức tính số loại phân tử được hình thành từ các loại đồng vị - Hóa học 10 chân trời sáng tạo
1. Kiến thức nền tảng cần nhớ
Đồng vị là các nguyên tử của cùng một nguyên tố, có cùng số proton (Z) nhưng khác số khối (A) → do khác số neutron.
Các đồng vị tham gia phản ứng hóa học như nhau, nhưng có thể tạo ra các phân tử khác nhau về khối lượng nếu chúng kết hợp theo cách khác nhau.
Phân tử hình thành từ các đồng vị gọi là phân tử đồng vị.
2. Công thức tổng quát
Nếu:
- Nguyên tố A có m đồng vị
- Nguyên tố B có n đồng vị
→ Số loại phân tử AB được hình thành là: m×n
Với phân tử dạng A₂ (hai nguyên tử A giống nhau), có m đồng vị của A, số loại phân tử là: m(m+1) / 2
Vì có thể ghép (A₁A₁, A₁A₂, A₂A₂, ..., AₘAₘ) và không phân biệt hoán vị (A₁A₂ ≡ A₂A₁)
Với phân tử dạng A₂B:
A có m đồng vị, B có n đồng vị
→ Số loại phân tử là: [m(m+1)/2] ×n
3. Ví dụ minh họa
Ví dụ 1. Clo có 2 đồng vị: Cl-35 và Cl-37. Có bao nhiêu loại phân tử Cl₂?
Vì Cl có 2 đồng vị → m = 2
⇒ số loại phân tử = [2(2+1)]/2=3
➡ Gồm: Cl-35–Cl-35, Cl-35–Cl-37, Cl-37–Cl-37
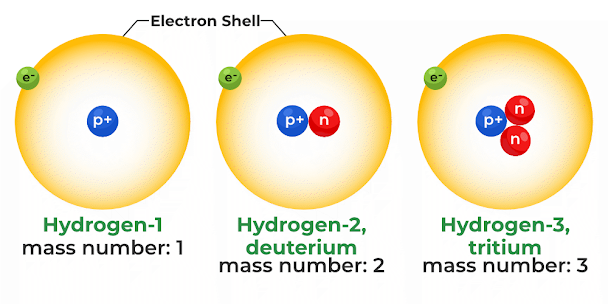
Ví dụ 2. Có 3 đồng vị của hiđro (H): Protium (H-1), Deuterium (D, H-2), Tritium (T, H-3).
Tính số loại phân tử có thể có của H₂.
m = 3 → Số loại phân tử = [3(3+1)] /2=6
➡ Các phân tử: H–H, H–D, H–T, D–D, D–T, T–T
Ví dụ 3. C có 2 đồng vị, O có 3 đồng vị → Tính số phân tử CO₂ tạo thành?
Phân tử CO₂ gồm 1C và 2O → Với O₂: 3 đồng vị → số tổ hợp:
[3(3+1)] /2=6
→ Tổng số loại CO₂: 2×6=12 loại phân tử.
4. Ghi nhớ nhanh công thức tính số loại phân tử được hình thành từ các loại đồng vị Hóa 10.
5. Phần tự luyện - Bài tập tính số phân tử tạo thành từ đồng vị
Bài 1. Nguyên tố X có 3 đồng vị, nguyên tố Y có 2 đồng vị. Hỏi có bao nhiêu phân tử XY được hình thành?
Bài 2. Hỏi có bao nhiêu phân tử có thể được hình thành từ NO nếu N có 2 đồng vị và O có 3 đồng vị?
Bài 3. Một nguyên tố A có 4 đồng vị. Có bao nhiêu phân tử A₂ có thể hình thành?
Giải nhanh.
Bài 1: 3×2=6 phân tử
Bài 2: 2×3=6 phân tử
Bài 3: [4(4+1)]/2=10 phân tử
6. Kết luận:
Việc vận dụng công thức để tính số loại phân tử được hình thành từ các đồng vị không chỉ giúp học sinh hiểu rõ bản chất của hiện tượng đồng vị trong hóa học, mà còn rèn luyện tư duy tổ hợp – một kỹ năng quan trọng trong các bài toán nâng cao và đề thi học sinh giỏi.
Qua bài học, chúng ta nhận thấy rằng chỉ với một số đồng vị hạn chế, các nguyên tố có thể tạo nên rất nhiều phân tử khác nhau, mở rộng cách hiểu về đa dạng cấu trúc và tính chất vật lý trong hóa học hiện đại. Ngoài ra, đây cũng là nền tảng để học sinh tiếp cận sâu hơn với các khái niệm như đồng vị phóng xạ, phân tử khối trung bình, và phân tích phổ khối trong chương trình học nâng cao và đại học sau này.
Xem thêm:
Thành phần của nguyên tử và Nguyên tố hóa học - Hóa học 10 Chân trời sáng tạo.
Bài tập thành phần cấu tạo của nguyên tử - Hóa học 10 Chân trời sáng tạo.
Công thức tính số loại phân tử được hình thành từ các loại đồng vị | Hóa Học 10
Các dạng bài tập về đồng vị hóa học.
Cấu trúc lớp vỏ electron của nguyên tử.
Hướng dẫn cách viết cấu hình Electron nguyên tử của 30 nguyên tố đầu tiên.
Nguyên lí Pauli | Cấu trúc lớp vỏ Electron của nguyên tử.
Quy tắc Hund | Cấu trúc lớp vỏ Electron của nguyên tử.
Hướng dẫn cách viết cấu hình electron nguyên tử | Hóa 10 Chân trời sáng tạo.
Bài tập thành phần của nguyên tử | Hóa học 10 chân trời sáng tạo.
Bài tập nguyên tố hóa học chương 1 cấu tạo nguyên tử | Hóa học 10 chân trời sáng tạo.
Bài tập tự luận cấu trúc lớp vỏ Electron của nguyên tử | Hóa học 10 chân trời sáng tạo.
Ôn tập chương 1 cấu tạo nguyên tử - phần bài tập tự luận.
Lý thuyết Hóa học 10 chương 1 Cấu tạo nguyên tử.
Hóa học 10 chân trời sáng tạo.
Luyện thi tốt nghiệp trung học phổ thông quốc gia môn Hóa học.














COMMENTS